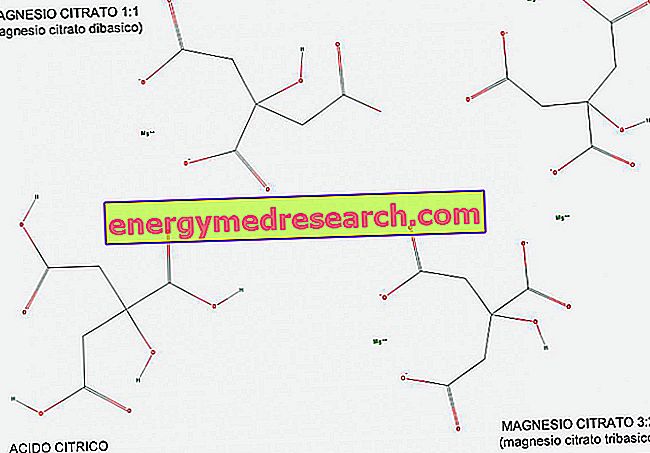
Un acid tribazic (sau triprotic) este un acid care posedă trei ioni de hidrogen care trebuie donați într-o reacție bazică acidă. Cu ajutorul figurii putem vedea cum acidul citric este un exemplu de acid tribazic, deoarece are trei grupări carboxilice COOH care pot da cu ușurință H hidrogen.
Citratul de magneziu există în proporție de 1: 1 (1 molecula de magneziu per moleculă de citrat) și în proporție de 3: 2 (3 molecule de magneziu la 2 molecule de citrat).
Citrat de magneziu 1: 1 se numește dibazic deoarece este o sare dibazică a acidului citric; de fapt, are 2 grupări bazice univalente (COO-) per moleculă, derivate din cele 2 grupări carboxilice care au renunțat la hidrogenul lor în timpul reacției.
Magneziu 3: 2, pe de altă parte, se numește tribazic deoarece are 3 grupări bazice univalente (COO-) per moleculă, derivate din cele 3 grupări carboxilice care au renunțat la hidrogenul lor în timpul reacției.
Citratul tribazic de magneziu este în mod evident mai bogat în magneziu (+ 42, 6% în greutate) decât citratul de magneziu dibazic; în plus, este mai alcalinizantă, deoarece poate accepta trei ioni de hidrogen H + împotriva celor doi acceptați de dibazic. Cu toate acestea, este mai puțin solubil în apă.



